Autophagie – ein Heilmittel für viele Krankheiten der heutigen Zeit?
„Autophagie – ein Heilmittel für viele Krankheiten der heutigen Zeit?“ ist eine Übersetzung des Artikels „Autophagy – a cure for many present-day diseases?“ von Dr. Jason Fung, M.D. erschienen auf Diet Doctor in in Cancer, Dementia, Diabetes, Heart disease, Intermittent fasting, Liver disease, PCOS / Fertility, Protein, The obesity epidemic
Vielen Dank für die Übersetzung, liebe Claudia Heine.
Autophagie – ein Heilmittel für viele Krankheiten der heutigen Zeit?
Autophagie, ein Reinigungsprozess der Zelle, wird aktiviert durch bestimmte Formen von metabolischem Stress, einschließlich Nährstoffmangel, Abschwächung des Wachstumsfaktors und Sauerstoffmangel. Selbst bei suboptimalen Bedingungen kann jede Zelle subzelluläre Teile abbauen und diese in neue Proteine oder Energie umwandeln, wie sie zum Überleben benötigt werden. Dies erklärt, warum mTOR und Autophagie in jedem Organismus von der Hefe bis zum Menschen gefunden werden.
Untersuchungen an Mutationen von unterschiedlichsten Lebewesen wie Hefe, Schleimpilzen, Pflanzen und Mäusen zeigen, dass die Zerstörung von an der Autophagie beteiligten Genen (ATG) in Tieren mit dem Leben kaum vereinbar ist. Das heißt, fast alles Leben auf der Erde kann nicht ohne Autophagie existieren.
Insulin und Aminosäuren sind (durch mTOR) die Hauptregulatoren von ATGs. Dies sind auch zwei unserer grundlegendsten Nährstoffsensoren. Wenn wir Kohlenhydrate essen steigt der Insulinspiegel. Wenn wir Protein essen, steigen sowohl Insulin als auch mTOR. Wenn Nährstoffsensoren Nährstoffe wahrnehmen, signalisieren wir unserem Körper zu wachsen. So stoppen Nährstoffsensoren die Autophagie, die in erster Linie ein kataboler Prozess ist (Abbau), im Gegensatz zu einem anabolen Prozess (Aufbau). Es gibt jedoch immer ein niedriges grundlegendes Level von Autophagie, da es als eine Art zelluläre Reinigungskraft fungiert.
Zelluläre Reinigung
Die Hauptaufgaben der Autophagie sind: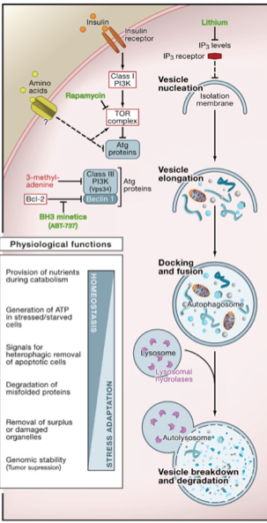
defekte Proteine und Organellen entfernen
verhindern abnormaler Proteinanhäufung
entfernen intrazellulärer Krankheitserreger
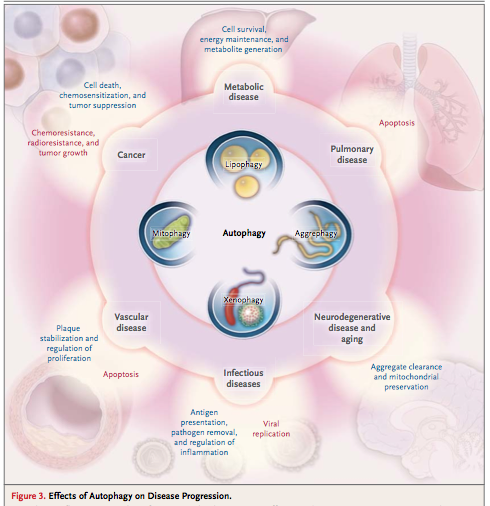
Diese Mechanismen sind beteiligt in vielen altersbedingten Krankheiten – Atherosklerose, Krebs, Alzheimer, neurodegenerative Erkrankungen (Parkinson).
Das zelluläre Kontrollsystem dient der Qualitätskontrolle der Proteine in unserem Körper.
Genetisch mutierte Mäuse, denen ATGs fehlen, entwickeln eine übermäßige Proteinanreicherung im Inneren der Zellen.
Die Folge sind beschädigte Proteine, die nicht abgebaut werden und sich anhäufen.
Es gibt einen verwandten Prozess namens Mitophagie, um die abnormalen Organellen (in diesem Fall Mitochondrien) zu eliminieren.
Autophagie – ein Tumorsuppressor?
Bei Krebs ist es allgemein anerkannt, dass Autophagie die Tumorinitiation unterdrücken kann. Da die Autophagie das Wachstum blockiert und den Abbau von Proteinen erhöht, ist dies durchaus sinnvoll. Zum Beispiel haben Krebszellen oft eine viel geringere basale Autophagie als normale Zellen. Viele der am besten untersuchten Onkogene und Tumorsuppressorgene sind eng mit der Autophagie verbunden.
Zum Beispiel blockiert das bekannte PTEN-Tumorsuppressor-Gen PI3K /Akt, wodurch die Autophagie aktiviert wird. Mutationen an PTEN, die bei Krebserkrankungen sehr häufig vorkommen, führen daher zu einer geringeren Autophagie und einem erhöhten Krebsrisiko. Es scheint jedoch ein zweischneidiges Schwert zu sein. Wenn der Krebs fortschreitet, kann Autophagie das Überleben von Krebs unterstützen, genauso wie sie allen Zellen hilft, in einer stressigen Umgebung zu überleben.
In Zeiten von Nährstoffmangel baut Autophagie Proteine zu Aminosäuren ab, die zur Energiegewinnung genutzt werden können. Krebs der so schnell wächst, dass seine eigene Blutversorgung nicht mehr ausreicht, kann so durch erhöhte Autophagie unterstützt werden, da diese viel benötigte Energie liefert und ihn im Umgang mit Stress unterstützen würde.
Neurodegenerative Erkrankungen
Der andere Bereich von großem Interesse sind die neurodegenerativen Erkrankungen Alzheimer, Parkinson und Chorea Huntington. Während sich diese alle unterschiedlich zeigen, Alzheimer mit Gedächtnisverlust und anderen kognitiven Veränderungen, Parkinson mit Verlust der willkürlichen Bewegung und Ruhetremor und Huntington mit unwillkürlichen Bewegungen, teilen sich alle eine pathologische Ähnlichkeit.
Alle diese Krankheiten sind durch einen übermäßigen Aufbau von Proteinen innerhalb von Neuronen gekennzeichnet, die zu Funktionsstörungen und letztendlich zu Krankheiten führen. 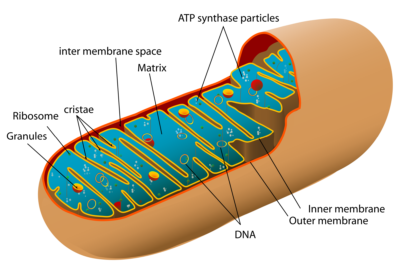 Daher kann das Versagen von Proteinabbauwegen eine sehr wichtige Rolle spielen. Die genaue Rolle der Autophagie bei diesen Erkrankungen muss jedoch noch bestimmt werden. Darüber hinaus deutet die zunehmende Forschung auch auf mitochondriale Funktionsstörungen als einen Schlüsselweg bei der Entwicklung neurodegenerativer Erkrankungen hin.
Daher kann das Versagen von Proteinabbauwegen eine sehr wichtige Rolle spielen. Die genaue Rolle der Autophagie bei diesen Erkrankungen muss jedoch noch bestimmt werden. Darüber hinaus deutet die zunehmende Forschung auch auf mitochondriale Funktionsstörungen als einen Schlüsselweg bei der Entwicklung neurodegenerativer Erkrankungen hin.
Studien an Menschen sind aufgrund der vielen sich überschneidenden Pfade schwierig. Der klarste Beweis kommt normalerweise von Medikamenten, durch die ein einzelner Pfad geändert werden kann. Die mTOR-Inhibitoren (Rapamycin, Everolimus) aktivieren die Autophagie, indem sie mTOR blockieren. mTOR ist ein Nährstoffsensor, vorwiegend für Aminosäuren. Wenn Proteine verzehrt werden, steigt der mTOR-Wert an. Wenn keine Nährstoffe aufgenommen werden, sinkt der mTOR-Wert und die Autophagie steigt an. Rapamycin blockiert mTOR und täuscht dem Körper vor, dass es keine Nährstoffe gibt, was die Autophagie erhöht.
Diese Medikamente werden hauptsächlich wegen ihrer immunsuppressiven Wirkung in der Transplantationsmedizin eingesetzt. Interessanterweise erhöhen jedoch die meisten Immunsuppressiva das Krebsrisiko, wo Rapamycin das Risiko nicht erhöht. Bei bestimmten seltenen Krebsarten haben mTOR-Inhibitoren krebshemmende Wirkungen gezeigt.
Metformin, ein Medikament, das häufig bei Typ-2-Diabetes eingesetzt wird, aktiviert auch Autophagie, aber nicht durch mTOR. Es erhöht AMPK, ein Molekül, das den Energiestatus der Zelle signalisiert. Wenn AMPK hoch ist, weiß die Zelle, dass sie nicht genug Energie hat und erhöht die Autophagie. AMPK erkennt das ADP / ATP-Verhältnis und kennt somit die zellulären Energieniveaus – ähnlich wie bei einer Tankanzeige, aber umgekehrt. Ist AMPK hoch, so ist der zelluläre Energiezustand niefrig. Hohe AMPK-Spiegel aktivieren direkt und indirekt die Autophagie, aber auch die mitochondriale Produktion.
Mitophagie
Mitophage ist das selektive Ansteuern defekter oder dysfunktionaler Mitochondrien. Dies sind die Teile der Zelle, die Energie produzieren – die Kraftwerke. Wenn diese nicht richtig funktionieren, dann zielt der Prozess der Mitophagie auf die Zerstörung ab. Zu den kritischen Regulatoren dieses Prozesses gehört das Tumorsuppressorgen PTEN. Dies mag negativ klingen, jedoch wid gleichzeitig zur Erhöhung der Mitophagie auch das Wachstum neuer Mitochondrien stimuliert.
AMPK zum Beispiel stimuliert sowohl die Mitophagie als auch das Wachstum neuer Mitochondrien – im Wesentlichen wird in einem Erneuerungsprozess altes Mitochondrium durch neues ersetzt: eine vollständige Erneuerung des Mitochondrien-Pools. Das alte, beschädigte Mitochondrium wird abgebaut und der Körper zum Aufbau neuer Mitochondrien angeregt. Dies ist einer der Gründe, warum Metformin allgemein als Anti-Aging-Präparat beworben wird – nicht so sehr wegen seiner Blutzucker-Wirkung, sondern vielmehr wegen seiner Wirkung auf AMPK und Autophagie.
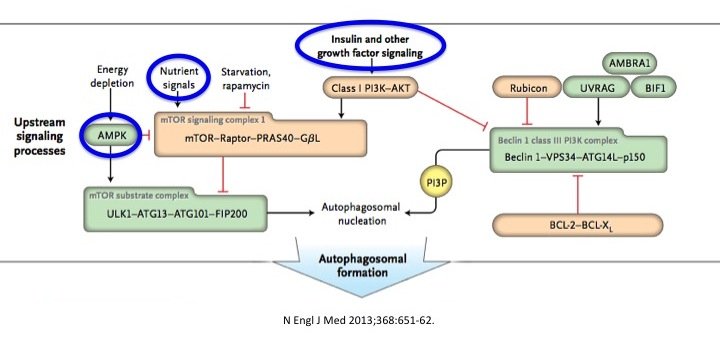
mTOR ist der zentrale Nährstoffsensor, der die Autophagie beeinflusst. mTOR analysiert die Signale von Insulin, Nährstoffen (Aminosäuren oder Nahrungsprotein) und der Brennstoffanzeige der Zelle, AMPK (die gesamte Energie einschließlich Fette), um zu bestimmen, ob sich die Zelle teilen und wachsen oder sich zurückbilden und in einen Ruhezustand übergehen soll. Überschüssige Nährstoffe – nicht nur Kohlenhydrate, sondern alle Nährstoffe – können das mTOR-System stimulieren und damit die Autophagie ausschalten, wodurch der Körper in einen Wachstumsmodus versetzt wird. Dies fördert das Wachstum der Zellen, was bei Erwachsenen normalerweise nicht gut ist.
Diese Signalwege sind für das Leben auf der Erde von zentraler Bedeutung, da sie die Verbindung zwischen Nährstoffzustand und Wachstum darstellen. Wenn bei Einzellern nicht genügend Nährstoffe vorhanden waren, gingen sie einfach in einen Ruhezustand über. Denken Sie an eine Hefe. Wenn es keine Nahrung gibt, trocknet sie einfach zu einer Spore aus. Wenn sie auf Wasser landet, blüht sie und beginnt zu wachsen. Der Schimmel sitzt in Ihrem Haus in einem ausgetrockneten, inaktiven Zustand. Wenn er auf Brot landet, beginnt er zu einem bekannten Schimmelpilz zu wachsen. Er wächst nur, wenn genügend Nährstoffe und Wasser vorhanden sind.
In einem mehrzelligen Organismus wird es viel schwieriger, die Verfügbarkeit von Nährstoffen und Wachstumssignalen zu synchronisieren. Wir sind darauf ausgelegt, tage- oder wochenlang ohne Nahrung zu leben – wir leben von der gespeicherten Nahrungsenergie in unserem Körperfett. Wenn die Nahrung jedoch knapp ist, möchten wir nicht schnell wachsen, und deshalb benötigen wir Nährstoffsensoren, die direkt mit den Wachstumspfaden verbunden sind. Die drei wichtigsten sind:
mTOR – empfindlich gegenüber diätetischem Protein
AMPK – „Umgekehrte Tankanzeige“ der Zelle
Insulin – empfindlich gegenüber Protein und Kohlenhydraten
Wenn diese Nährstoffsensoren eine geringe Nährstoffverfügbarkeit feststellen, sagen sie unseren Zellen, dass sie aufhören sollen zu wachsen und unnötige Teile abbauen – das ist die Selbstreinigungskraft der Autophagie.
Wenn wir Krankheiten mit übermäßigem Wachstum haben, können wir die Wachstumssignale durch Aktivierung dieser Nährstoffsensoren reduzieren. Diese Liste von Krankheiten umfasst Fettleibigkeit, Typ-2-Diabetes, Alzheimer, Krebs, Atherosklerose (Herzinfarkt und Schlaganfall), polyzystisches Ovarialsyndrom, polyzystische Nierenerkrankung und Fettleber, unter anderem. All diese Krankheiten sind für eine Ernährungsintervention geeignet.
Neuigkeiten

Sie möchten Experten der LCHF-Ernährung erleben? Das Who is Who der Low-Carb-Szene trifft sich traditionell im Februar in Düsseldorf. Es findet stets ein reger Austausch statt, der alle bereichert. Sie haben Lust auf die große LCHF-Familie? Dann kommen Sie zum Low Carb – LCHF Kongress. Um einen Eindruck vom Kongress zu gewinnen können Sie sich kostenlos Vorträge auf unserem YouTube-Kanal ansehen.
Sie möchten jeden Tag ein kleines Häppchen Wissen bequem per Audio-Datei hören? Dann ist unser 365-Tage -Audioprogramm perfekt für Sie. Starten Sie ab sofort täglich mit Leichtigkeit gesund durchs Leben – das 365 Tage-Programm für 198 Euroals Einmalzahlung oder Sie buchen für 19,80 Euro monatlich mit der Möglichkeit, das Abo jederzeit zu kündigen. Das Abo endet nach 12 Monaten automatisch. Hier
Sie möchten das Neueste aus dem Bereich Gesundheit und Ernährung erfahren? Prima, dann abonnieren Sie unseren Newsletter. Wenn Sie keine neuen Posts verpassen möchten, dann abonnieren Sie unseren Blog hier.
www.LCHF-Deutschland.de und LCHF Deutschland Akademie und LCHF Kongress und LCHF Magazin
Titelbild: claudioventrella by Envato
Bilder im Text: Jason Fung / Diet Doctor.com und Fotolia.com






Sandra 16. Februar 2020
Also ich habe von dem Text echt nicht viel verstanden 🙁
Schade, aber dank dr. Google habe ich was ganz einfaches und simples gefunden das ich kapiert habe…
https://www1.wdr.de/mediathek/video-autophagie-zellen-verwerten-ihren-muell-100.html
ein Video von WDR und jetzt wurde mir der ganz lange Text klar…FASTEN
Petra 16. Februar 2020
Sehr schwierig zu verstehen. Zuviele Abkürzungen . Sehr technisch erklärt.
Margret Ache 17. Februar 2020
Vielen Dank für die Rückmeldung. Wir werden versuchen bei Übersetzungen noch eine leicht verständliche Zusammenfassung zu machen.