„Das Insulin und die Fettleber“ ist eine Übersetzung des Artikels „Insulin och fettlever“ von Jason Fung, erschienen auf der Website des Diet Doctors Andreas Eenfeldt: https://www.dietdoctor.com/insulin-fatty-liver-disease und hier: http://www.kostdoktorn.se/insulin-och-fettlever.
Dr. Jason Fung ist ein weltweit anerkannter Experte auf dem Gebiet des Intermittierenden Fasten und der LCHF-Ernährung. In diesem Artikel beleuchtet er die Geschichte der Fettleber und was sie mit dem Insulin zu tun hat.
Vielen Dank für die Übersetzung, lieber Bernd Schwerdt.
Das Insulin und die Fettleber
Im Jahr 1890 begann Dr. Alfred Fröhlich von der Universität Wien die hormonell bedingten Ursachen der Fettleibigkeit zu untersuchen. Er beschrieb einen jungen Burschen, der in kurzer Zeit sehr stark zugenommen hatte und bei dem schließlich eine Schädigung in der Hypothalamusregion (Der Hypothalamus ist ein lebenswichtiger Teil des Zwischenhirns und dient als oberstes Regulationszentrum für alle vegetativen und endokrinen Vorgänge. )des Gehirns festgestellt wurde. Später wurde bestätigt, dass Schäden im Hypothalamus mit unaufhaltsamen Gewichtszunahme einhergehen.
Bei Ratten und anderen Tieren führen Schäden am Hypothalamus im Experiment zu maßlosem Appetit und Fettleibigkeit. Aber die Forscher fanden schnell auch etwas Anderes. Alle jene Tiere mit Fettleibigkeit hatten einen charakteristischen Leberschaden, der manchmal zur vollständig zerstörten Leber führte. Indem man Mäuse mit Anlage zu Fettleibigkeit näher betrachtete, entdeckte man vergleichbare Veränderungen der Leber. Das ist doch komisch, dachte man. Was hat die Leber mit Fettleibigkeit zu tun?
Dr. Samuel Zelman entdeckte im Jahre 1952 als Erster eine Verbindung zwischen Lebererkrankung und Fettleibigkeit. Er beobachtete eine Fettleber bei einer Pflegehelferin, die mehr als 20 Flaschen Coca-Cola am Tag trank. Bei Alkoholabhängigen waren entsprechende Komplikationen bekannt, aber diese Patientin trank keinen Alkohol. Dass Fettleibigkeit vergleichbare Leberschäden zur Folge hatte, wusste man zu dem Zeitpunkt noch nicht.
Basierend auf den Daten aus den Tierstudien suchte Zelman im folgenden Jahr 20 weitere übergewichtige Patienten, die eine Fettleber hatten, die nicht auf Alkohol beruhten. Auffällig war, dass alle eine kohlenhydratreiche Kost bevorzugten.
Die Fettleber bei Patienten, die keine Alkoholiker sind

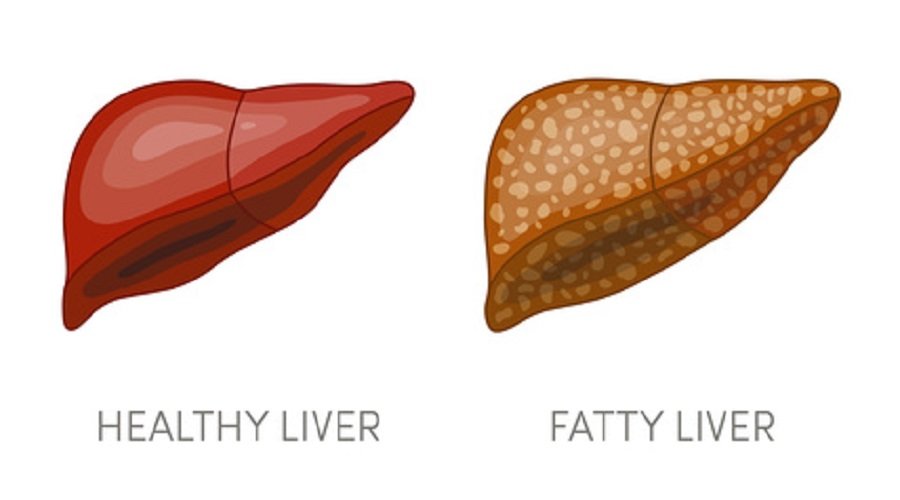
Leber normal – Fettleber
Ungefähr 30 Jahre später, im Jahre 1980, beschrieben Dr. Ludwig und seine Kollegen an der Mayo-Klinik eigene Erfahrungen. Bei 20 Patienten hatte sich eine Fettleber gebildet, vergleichbar mit der bei Alkoholikern, obwohl sie keinen Alkohol tranken. Diese bis dahin namenlose Krankheit erhielt den englischen Namen Non Alcoholic Steatohepatitis (NASH), der heute noch verwendet wird. Erneut wurde klinisch der Zusammenhang von Fettleibigkeit und Übergewicht zu Krankheiten wie Diabetes untersucht. Außer vergrößerten Lebern fanden sich auch Beweise von Leberschädigungen. Wenn eine Fettinfiltration offenbar ist, sich aber kein Nachweis für einen Leberschaden findet, wendet man den Terminus Non-Alacoholic-Fatty-Liver-Disease (NAFLD), deutsch: Nicht alkoholische Fettleber (NAFL) an.
Diese Entdeckung entlastete Patienten von den wiederholten Unterstellungen der Ärzte, dass sie über ihren Alkoholkonsum unwahre Angaben machten. Dr. Ludwig schrieb, dass Ärzte dadurch von den Peinlichkeiten (oder schlimmer) verschont wurden, die aus diesen Diskussionen entstehen konnten. Bestimmte Dinge im Leben verändern sich nie. Heute, wenn sich Patienten mit dem Abnehmen „Iss weniger, beweg dich mehr“ schwer tun, unterstellen die Ärzte den Patienten zu schummeln, anstatt die bittere Wahrheit zu akzeptieren, dass diese Kost ganz einfach nicht funktioniert. Dieses uralte Spiel nennt sich „Das Opfer ist selbst schuld“.
Mit den neuen Erkenntnissen bei NAFLD bestätigte die Forschung eine nahestehende Kopplung zwischen Fettleibigkeit, Insulinresistenz und Fettleber. Bei Individuen mit Fettleibigkeit war eine Fettleber fünf- bis zehnmal üblicher. Bei Typ-2-Diabetes-Patienten haben etwa 85% eine Fettleber. Auch ohne Diabetes haben Personen mit einer Insulinresistenz erhöhte Leberfettwerte. Diese drei Krankheiten haben einen ganz deutlichen Zusammenhang. Findet man eine davon, findet man meist auch die anderen.
Hepatische Steatose, also die Ansammlung von Fett in der Leber, wo es nicht hingehört ist demzufolge eines der wichtigsten Anzeichen einer Insulinresistenz. Der Grad der Insulinresistenz steht in direkter Beziehung zur Menge Fett in der Leber. Erhöhte Werte von Alanin-Transaminasen, ein Blutmarker für Leberschäden, steht bei fettleibigen Kindern in direktem Zusammenhang zu Insulinresistenz und der Entwicklung von Typ-2-Diabetes. Auch unabhängig von Fettleibigkeit korreliert der Grad der Fettleber mit Prä-Diabetes, Insulinresistenz und der verminderten Funktion der Betazellen.

Anstieg der Krankenhauseinweisungen wegen Fettleber.
Die Zunahme von NAFLD, sowohl bei Kindern als auch bei Erwachsenen ist alarmierend. Sie ist die Ursache von unnormalen Leberenzymen und chronischen Lebererkrankungen in der westlichen Welt. NAFLD betrifft schätzungsweise ⅔ aller Personen mit Fettleibigkeit. Für die NASH (Leberentzündung) sieht es noch schlechter aus. Man geht davon aus, dass die NASH die Hauptursache für die Leberzirrhose in der westlichen Welt sein wird. Es gibt schon ganz deutliche Zeichen für den Bedarf an Lebertransplantationen mit stark steigender Tendenz innerhalb dieses Jahrzehnts. In Nordamerika erwartet man eine Ausbreitung der NASH von 23 %.
Eine erschreckende Epidemie. Innerhalb nur einer Generation hat sich diese Krankheit, die gänzliche unbekannt war und nicht einmal einen Namen hatte zur häufigsten Ursache von Leberkrankheiten in Nordamerika entwickelt. Gänzlich unbekannt hat sie sich zum Weltrekordhalter in der höchsten Gewichtsklasse entwickelt, der Rocky Balbao der Leberkrankheiten.
Fettleber – das grundlegende Problem
Die Leber ist die Zentrale für die Lagerung und Produktion von Energie aus der Ernährung. Nach Aufnahme durch den Darm werden die Nährstoffe direkt durch den Portalkreislauf an die Leber geliefert. Nachdem das Körperfett grundsätzlich die Methode zur Lagerung der Energie aus der Nahrung ist, ist es nicht verwunderlich, dass Krankheiten der Fetteinlagerung die Leber beeinträchtigen.
Das Insulin drückt die Glukose in die Leberzellen und füllt die Leber allmählich. Die Leber wandelt durch die Lipogenese die überflüssige Glukose in Fett um, die Lagerungsform von Energie aus der Nahrung. Zu viel Glukose und zu viel Insulin über einen langen Zeitraum führen schließlich zur Fettleber.
Insulinresistenz ist ein Überschwemmungsproblem, da die Glukose nicht ein die überfüllten Zellen gelangen kann. Fettleber als Manifestation der überfüllten Zellen schafft Insulinresistenz. Der Zyklus geht weiter:
- Hyperinsulinämie schafft Fettleber
- Fettleber verursacht Insulinresistenz
- Insulinresistenz wiederum erhöht die Hyperinsulinämie
- Hyperinsulinämie verursacht Insulinresistenz und ist der Auslöser des Teufelskreises.
Fettleber führt zu Typ-2-Diabetes
Die Fettleber hat einen direkten Zusammenhang über alle Stadien von der Insulinresistenz zur Prä-Diabetes, vollständigen Diabetes, unabhängig von Fettleibigkeit. Dieser Zusammenhang besteht bei allen Volksgruppen, unabhängig davon, ob es sich um Asiaten, Weiße oder Afroamerikaner handelt.
Der entscheidende Faktor, der notwendig ist, um eine Insulinresistenz zu entwickeln, ist nicht die Fettleibigkeit, sondern das Leberfett, wo keines sein sollte. Das ist der Grund, dass es untergewichtige Patienten gemäß BMI gibt, die trotzdem Typ-2-Diabetes bekommen. Diese Patienten werden oft „schlanke Diabetiker“ genannt, oder TOFI (thin outside fat inside). Das Körpergewicht spielt eine kleinere Rolle, als das Fett um Bauch und Leber. Dieses Bauchfett, eher als die generelle Fettleibigkeit charakterisiert das metabolische Syndrom und Typ-2-Diabetes.
Das Fett unter der Haut, sogenanntes subkutanes Fett erhöht das Körpergewicht und den BMI, hat aber nur minimale Konsequenzen für die Gesundheit. Vom kosmetischen Standpunkt ist es unerwünschtes Körperfett, ist aber andererseits ungefährlich für den Stoffwechsel. Das kann man leicht erkennen, in Stoffwechselstudien nach Fettabsaugungen, einer der gewöhnlichsten Eingriffe unter Narkose in den USA. Über 400.000 Eingriffe werden jedes Jahr in den USA durchgeführt.
Das chirurgische Entfernen größerer Mengen subkutanen Fetts vermindert das Körpergewicht, BMI, Taillenumfang und das Hormons Leptin. Doch die Stoffwechselparameter, sogar bei der Entfernung von 10 kg subkutanen Fetts verbessern sich nicht. Es gibt keine messbaren Verbesserungen des Blutzuckers, der Insulinresistenz, Entzündungsmarker oder im Cholesterinprofil. Das Ausbleiben von Vorteilen geschieht trotz vergleichbarer Fettminderungen verglichen mit Fettabnahme durch Abnehmprogramme mit Ernährung.
Im Gegensatz dazu erzielt eine Abnahme durch Ernährungsveränderung eine deutliche Verbesserung sämtlicher Stoffwechselparameter. Konventionelle Abnehmmethoden vermindern das subkutane Fett, viszerales Fett und das Fett in der Leber, während die Fettabsaugung lediglich das subkutane Fett vermindert.
Das viszerale Fett ist ein viel besserer Prädiktor für Diabetes, hohes Cholesterin und Herzkrankheiten verglichen mit dem totalen Körperfett. Trotzdem existiert noch immer ein entscheidender Unterschied zwischen Fett in den Organen und Fett um die Organe herum. Das chirurgische Entfernen von Fett an den Organen bringt keine Vorteile beim Stoffwechsel.
Fettleber und Insulinresistenz
 Die Entwicklung einer Fettleber ist ein entscheidendes Sprungbrett für eine erhöhte Insulinresistenz, die das grundsätzliche Problem bei Typ-2-Diabetes ist. Mit ausreichend verfügbarer Glukose als Substrat treibt das Insulin die neue Fettproduktion an und schließlich die Fettleber. Das Insulin versucht vergeblich mehr Glukose in die überschwemmten Leberzellen zu verschieben, allerdings ohne Erfolg, wie in einem überschwemmten U-Bahnwaggon. Das ist die Insulinresistenz in der Leber. Das Fett in anderen Organen als der Leber spielt auch eine entscheidende Rolle bei Krankheiten. Üblicherweise befindet sich nicht viel Fett in den Organen, aber das Fett führt zu den meisten Komplikationen bei Fettleibigkeit (18). Das schließt das Fett in der Leber ein, aber auch Fett, das sich in den Skelettmuskeln und der Bauchspeicheldrüse befindet.
Die Entwicklung einer Fettleber ist ein entscheidendes Sprungbrett für eine erhöhte Insulinresistenz, die das grundsätzliche Problem bei Typ-2-Diabetes ist. Mit ausreichend verfügbarer Glukose als Substrat treibt das Insulin die neue Fettproduktion an und schließlich die Fettleber. Das Insulin versucht vergeblich mehr Glukose in die überschwemmten Leberzellen zu verschieben, allerdings ohne Erfolg, wie in einem überschwemmten U-Bahnwaggon. Das ist die Insulinresistenz in der Leber. Das Fett in anderen Organen als der Leber spielt auch eine entscheidende Rolle bei Krankheiten. Üblicherweise befindet sich nicht viel Fett in den Organen, aber das Fett führt zu den meisten Komplikationen bei Fettleibigkeit (18). Das schließt das Fett in der Leber ein, aber auch Fett, das sich in den Skelettmuskeln und der Bauchspeicheldrüse befindet.
Die Fettleber entsteht 10 oder mehr Jahre vor einer Diabetesdiagnose. Das Entstehen des metabolischen Syndroms folgt einem konsequenten Weg. Gewichtszunahme, auch wenn es nur 2 kg sind, sind die ersten nachweisbaren Abnormitäten, gefolgt von niedrigen HDL-Cholesterinwerten. Hoher Blutdruck, Fettleber und hohe Triglyceride folgen ungefähr zur gleichen Zeit. Das allerletzte Symptom sind dann die hohen Blutzuckerwerte. Diese entdeckt man erst spät beim metabolischen Syndrom.
West-of-Scotland-Studien bestätigen, dass Fettleber und erhöhte Werte der Triglyceride 18 Monate vor einer Typ-2-Diabetes-Diagnose vorhergehen. Die Triglyceridwerte steigen ein halbes Jahr vor der Diagnose an. Das ist der Beweis dafür, dass das Speichern von Leberfett entscheidend für die Entstehung einer Insulinresistenz und außerdem der Auslöser für eine Typ-2-Diabetes ist.
 Obwohl im Prinzip alle Patienten mit Insulinresistenz eine Fettleber haben, ist das Gegenteil nicht richtig. Nur eine Minorität von Patienten mit einer Fettleber hat ein metabolisches Syndrom. Das deutet darauf hin, dass die Fettleber einer Insulinresistenz vorangeht, welches mit dem Überschwemmungsparadigma übereinstimmt. Im Laufe der Jahre führt ein chronischer Überschuss an Insulin zur Speicherung von mehr und mehr Leberfett, welches weitere Einlagerungen von Glukose verhindert. Die überfüllte Fettleber schafft eine Insulinresistenz. Bei Patienten mit Typ-2-Diabetes besteht ein starker Zusammenhang mit der Menge an Leberfett und der Insulindosis, die erforderlich ist und reflektiert eine noch größere Insulinresistenz. Kurz gesagt, je fetter die Leber ist, desto mehr Insulinresistenz.
Obwohl im Prinzip alle Patienten mit Insulinresistenz eine Fettleber haben, ist das Gegenteil nicht richtig. Nur eine Minorität von Patienten mit einer Fettleber hat ein metabolisches Syndrom. Das deutet darauf hin, dass die Fettleber einer Insulinresistenz vorangeht, welches mit dem Überschwemmungsparadigma übereinstimmt. Im Laufe der Jahre führt ein chronischer Überschuss an Insulin zur Speicherung von mehr und mehr Leberfett, welches weitere Einlagerungen von Glukose verhindert. Die überfüllte Fettleber schafft eine Insulinresistenz. Bei Patienten mit Typ-2-Diabetes besteht ein starker Zusammenhang mit der Menge an Leberfett und der Insulindosis, die erforderlich ist und reflektiert eine noch größere Insulinresistenz. Kurz gesagt, je fetter die Leber ist, desto mehr Insulinresistenz.
Im Gegensatz dazu sind die Insulinwerte bei Typ-1-Diabetes-Patienten extrem niedrig und die Werte des Leberfetts niedriger als normal. Das ist ein starker Beweis dafür, dass das Insulinniveau ein Schlüsselfaktor für die Entstehung von der Fettleber ist. Insulin treibt die Fettproduktion in der Leber und niedrige Insulinniveaus führen zu weniger Fett in der Leber.
Jason Fung
Hier können Sie sich für einen Monat kostenlos auf der Mitgliederseite von Diet Doctor
anmelden: https://www.dietdoctor.com/become-member
Der Low Carb – LCHF Kongress

Im Februar 2019 treffen sich namhafte Experten und Gesundheitsinteressierte zum Low Carb – LCHF Kongress in Düsseldorf.
Der Kongress ist eine attraktive Plattform für alle Low Carb – Ernährungsformen. Diese Ernährung stellt eine wesentliche Voraussetzung dar, um mit Leichtigkeit gesund durchs Leben gehen zu können.
Bereits am Freitag, den 22. Februar 2019 findet ab 18.00 Uhr ein Come together im Restaurantbereich statt. Mit Zeit zum Kennenlernen und Austausch der Kongressteilnehmer, Referenten und Aussteller.
Der Kongress beginnt am Samstag, den 23.02.2019 um 8.30 Uhr und endet am Sonntag, den 24.02.2019 gegen 16.00 Uhr. Sie zahlen 330,00 Euro Teilnehmergebühren inkl. Kongressjournal, zwei Mittagessen und Pausengetränke, Low Carb – Snacks sowie einer Tasche mit vielen weiteren Informationen. Studenten erhalten einen Sonderpreis von 200,00 Euro.
Die LCHF Deutschland Akademie wird mit einem Info-Stand zu dem aktuellen Kursangebot vertreten sein.
Wir freuen uns, Sie am 23. und 24. Februar 2019 in Düsseldorf zu treffen. Weitere Informationen finden Sie hier: http://low-carb-lchf-kongress.de/
Neuigkeiten
Sie möchten täglich das Neueste aus dem Bereich Gesundheit und Ernährung erfahren? Sie möchten kein Rezept versäumen? Prima, dann abonnieren Sie unseren Blog hier: https://lchf-deutschland.de/service/blog-abonnieren/
GANZ NEU! Sie können sich zu unserem Newsletter anmelden. Welche Infos Sie bekommen und wie oft er erscheint, erfahren Sie auf der Anmeldeseite!
Wir freuen uns sehr über neue Abonnenten!
https://lchf-deutschland.de/service/newsletter/
www.LCHF-Deutschland.de
Bildrechte: https://www.dietdoctor.com/ und Fotolia.com